状态方程
状态方程为本构关系,用于描述密度和内能与两个热力学基本变量压力和温度之间的关系。
Simcenter STAR-CCM+ 提供以下选项:
恒密度
其中, 为常数。
多项式密度
对于气体、液体和固体,密度可按多项式的形式指定为温度 的函数。温度范围可以细分为多个间隔,每个都具有自己的多项式函数:
其中, 为多项式系数。
理想气体
理想气体定律将密度表示为温度和压力的函数:
- 为压力
- 为单位气体常数
- 为通用气体常数 [8314.4621 J/kmol K]
- 为分子量
实际气体
在高压和低温条件下,实际气体的 p-v-T 行为与理想气体方程预测的行为有所偏差。这一行为变化是由于随着气体密度增加,气体分子占据了总体积的大部分。此外,分子间引力变得越来越重要。
- Van der Waals
-
van der Waals 方程由以下公式给出:
(673)Van der Waals 将理想气体关系中的单位体积 替换为 ,以考虑气体颗粒占据的体积,同时将压力替换为项 。常数 为颗粒的本身体积,常数 用于衡量引力。
常数 和 基于实验观察结果计算,在 p-v 空间中,在临界状态下( 且 ),临界等温 ,斜率为零并且具有拐点。因此,存在以下等式:
(674)和
(675)从而获得 和 的以下表达式:
(676)通过上述方程,可根据临界压力 和临界温度 的实验测量值确定 和 。
- Peng-Robinson
-
Peng-Robinson 方程由以下公式给出:
(677)其中, 为单位体积。
函数 由以下公式给出:(678)其中, 为折算温度, 为气体的离心因子。
常数为:
(679)
- Redlich-Kwong
-
Redlich-Kwong 方程由以下公式给出:
(680)且(681)
- Soave-Redlich-Kwong
- Soave 修正了 Redlich-Kwong 方程,将 Eqn. (681) 的分母中的
幂替换为不同的温度相关表达式 [210]。此修正改进了液体密度和汽-液平衡的预测,如下所示: (682)函数 为:(683)且(684)
- 已修正的 Soave-Redlich-Kwong 模型
- Graboski 和 Daubert 修正了 Soave-Redlich-Kwong 模型,以改进其涉及非极性分子 [173] 和 [174] 的相平衡计算的行为。所有方程仍与 Soave-Redlich-Kwong 模型相同,唯一区别为函数
更改为: (685)
- 平衡空气
- 对于高温下的空气,分子离解、内能激励和电离效应变得明显。
在这些效应的时间尺度比流的时间尺度短得多的情况中,可以按平衡方式处理这些效应。在这种情况下,流体属性(如密度、比热和传输属性)将变为两个热力学变量的表达式。这些表达式通常采用曲线拟合形式,考虑了在高温下出现的化学反应和能量模式。尤其是,使用了 Gupta 等人的 [176] 提出的曲线拟合。这些曲线拟合将可压缩性因子、比热、焓、粘度和导热率指定为温度与压力的函数。曲线拟合适用于低于 30,000 K 的温度和介于 10-4 和 102 个大气压之间的压力。
平衡空气状态方程将可压缩性因子作为场函数提供。在此模型上下文中,可压缩性因子表示空气的未离解分子量与平均分子量之比 [176]:
(686)其中, 表示未离解空气的分子量, 表示给定温度和压力下的空气平均分子量。由于平均分子量为成分的函数,因此可压缩性因子可用于衡量空气中的离解程度,值越高,表示离解和电离程度越大。
热非平衡
对于气体,内能包含了平移、旋转、振动和电子模式。在平衡状态下,可通过单个特征温度充分描述这些能量模式。在热非平衡状态下,平移和旋转能量模式由一个温度描述,而振动和电子能量模式由额外的振动-电子温度描述。振动-电子温度通过求解额外的能量方程确定,该方程描述了振动-电子能量的守恒。Gnoffo 等人的 [172] 提出了此方程,Lockwood [192] 将其简化为非电离流体:
振动-电子能量和平移-旋转能量的交换通过松弛项进行建模。在 Gnoffo 等人的 [172] 提出了此松弛并提供了简化,以便减少计算中包含的组分相关参数:
要描述振动-电子焓和温度之间的关系,必须指定振动比热。此振动比热通过同时设置总比热和平移 - 旋转比热指定。对于此模型,平移 - 旋转能量模式假设为全激励 ,因此平移 - 旋转比热恒定 。指定这两个值后,振动比热和焓由 [172] 给出:
IAPWS-IF97
使用 IAPWS-IF97(水与蒸汽特性国际协会,行业规定 1997)的模型,可以运行液态水或气态蒸汽的模拟。
此类模型包含密度和其他热力学属性的计算。IAPWS-IF97 为比吉布斯自由能 提供了基本多项式方程。单位体积、内能、熵、焓、热容和声速均可通过该基本方程,使用无量纲吉布斯自由能及其导数 [182] 的适当组合推导得出。
根据吉布斯自由能,Simcenter STAR-CCM+ 中的 IAPWS-IF97 模型仅适用于特定范围的温度和压力。这些范围在区域示意图中表示 [182],这些区域实质上代表了水与蒸汽的各个相。
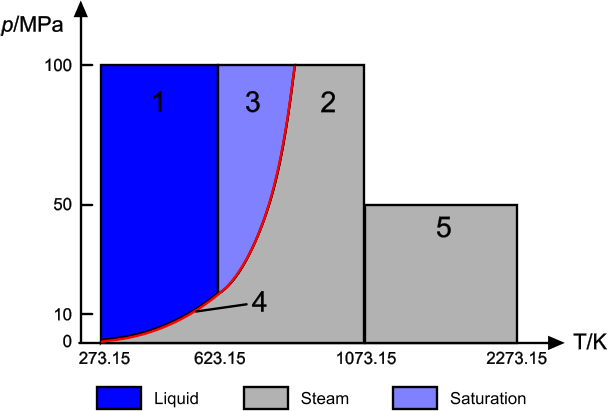
下表列出了区域示意图的各个组成部分以及它们如何与 Simcenter STAR-CCM+ 中的 IAPWS-IF97 模型搭配使用。
| 组成部分 | 有效范围 | STAR-CCM+ 模型 | |
|---|---|---|---|
| 区域 1(液体) | 273.15 K ≤ T ≤ 623.15 K | p ≤ 100 MPa | IAPWS-IF97(水) |
| 区域 2(蒸汽) | 273.15 K ≤ T ≤ 1073.15 K | p ≤ 100 MPa | IAPWS-IF97(蒸汽) |
| 区域 3(饱和) | Simcenter STAR-CCM+ 不支持此相区域。 | ||
| 边界 4 | 此边界的一侧为液体与饱和,另一侧为蒸汽。 | ||
| 区域 5(蒸汽) | 1073.15 K < T ≤ 2273.15 K | p ≤ 50 MPa | IAPWS-IF97(蒸汽) |
过热液体的焓 和过冷蒸汽的焓 分别计算如下:
其中:
- 为饱和温度
- 下标 和 分别指区域 1 和区域 2。
多组分气体
对于使用 Peng Robinson、Soave-Redlich-Kwong 或已修正的 Soave-Redlich-Kwong 方程的多组分气体, 和 基于对组分 的几何和算术求和:
其中, 为摩尔分数。