腐蚀
Simcenter STAR-CCM+ 中的电动势模型有助于了解和预测腐蚀的影响。
对于易于腐蚀的金属结构,挑战在于通过防止腐蚀最大程度地延长结构的设计寿命。 能够使用 Simcenter STAR-CCM+ 了解和预测腐蚀行为,就可以比较各种防腐蚀方法,为每种特定情景(即使具有复杂的几何)选择最佳方案。
防止腐蚀的一种方法是使用阴极保护。 阴极保护的概念很简单。 但是,找到最佳保护等级却比较复杂。 阴极保护不足将导致腐蚀。 过度保护可能会导致负面影响,如氢脆,这会削弱高强度钢的强度,增加结构断裂的可能性。
可以使用 Simcenter STAR-CCM+ 优化防腐蚀的牺牲阳极的位置和尺寸。 此过程确保了结构受到的阴极保护等级能够最有效地延长结构寿命。 模拟结构的阴极保护还可以防止昂贵阳极的不必要浪费,因此极具经济效益。
可以使用 Simcenter STAR-CCM+ 中的腐蚀模型对以下对象上的阴极保护进行建模:
- 船体
- 石油钻机和燃气管道
- 桥梁
- 钢筋混凝土
- 地下结构
要对腐蚀建模,按照电化学表面反应建模中的步骤操作。
什么是腐蚀?
腐蚀是一种电化学过程,当金属发生反应以形成比其纯元素状态更稳定的化合物时,将自然发生腐蚀。 在腐蚀过程中,金属和电解质之间的交界面处将发生很多电化学表面反应。 请参见电化学表面反应。
金属原子失去电子,成为可溶于电解质的离子。 金属失去电子的反应称为氧化 — 阳极反应就是一个示例。 以下反应显示了铁的氧化:
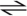
电解质接受来自金属的电子并形成离子。 物质接受电子的反应称为还原 — 阴极反应就是一个示例。 以下反应显示了水的还原:
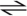
腐蚀过程中产生的离子将形成化合物,这些化合物在大部分情况下可溶于电解质。 腐蚀速率取决于金属和电解质之间交界面处的电势下降。 总体而言,腐蚀会导致金属分解,削弱金属结构并缩短其使用寿命。
在下图中,铁 在水 和氧气 的作用下发生腐蚀,失去电子 ,形成铁离子 。 水和氧气接受来自铁的电子,形成氢氧离子 :
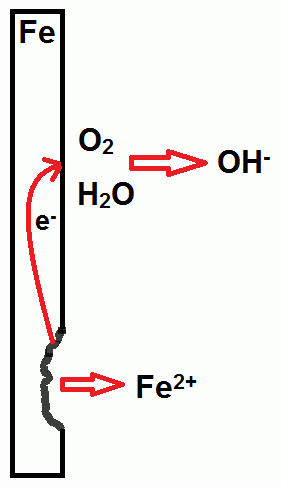
防止腐蚀的一种方法是使用阴极保护。
什么是阴极保护?
阴极保护是一种防止金属腐蚀的过程,通过创建受保护金属将在其中形成阴极的电化学电池实现。
可采用几种方法来创建用于阴极保护的电化学电池,包括:
- 从电源主动给金属施加直流电流
- 使用牺牲阳极
使用牺牲阳极
将牺牲阳极用于阴极保护时,金属阳极将连接到需要保护的金属结构。 阳极由平衡电势大于金属结构的金属制成。 由于这些阳极的作用是保护金属,因此阳极附近的电解质电势大于金属结构附近的电解质电势。 这种电势差导致离子流从阳极流向金属结构。 阳极处产生离子和电子,离子流过电解质,而电子流过金属电路。 然后离子和电子在阴极处重新结合。 由于金属的导电率较高,因此金属电路的电势下降通常远远小于电解质的电势下降。
提供给金属结构的电流可以防止金属结构发生氧化。
要对阴极保护建模,按照电化学表面反应建模中的步骤操作。